慢性病资讯
拒绝非酒精性脂肪“肝”扰,岩藻黄素为“肝脏健康”提供专业守护
2024-02-21 09:31 来源:新营养

天猫健康《2023健康年度词》[1]数据显示在过去的一年,“90后”对“小心肝”的关注度持续上涨,超过45%的护肝片被该群体包揽,大部分人是集中在凌晨时分进行下单,保肝护肝被越来越多的年轻人纳入日常保健计划。
目前国内“蓝帽子”产品市场需求聚焦在熬夜加班、喝酒应酬等场景,针对化学性肝损伤具有辅助保护功能。但随着肥胖症的日趋增多,2型糖尿病和代谢综合征的流行,我国非酒精性脂肪性肝病(Non-alcoholic fatty liver disease,NAFLD)发生率呈现明显上升态势,对全民身体健康产生了严重威胁。因此一款来自海洋生物活性成分——岩藻黄素(Fucoxanthin)在市场中走红,为开发差异化的养肝护肝类产品提供了创新要素。
1. “隐形杀手”:非酒精性脂肪性肝病(NAFLD)
肝脏是人体的劳模器官,每天就发生着1500种以上的化学反应,在体内发挥代谢、解毒、消化等多种功能。就如人不能一直工作一样,如果肝脏长期处于“永动机”状态,也会不堪重负,容易造成肝细胞结构或功能的异常——肝损伤(Hepatic injury)。
肝损伤的形成原因较为复杂,受病毒性、酒精性、脂肪性、药物性及自身免疫性等因素的影响。由于生活方式以及饮食结构的改变,非酒精性脂肪性肝病(NAFLD)已经成为当今社会最常见慢性病之一,发病群体渐趋年轻化。
《Journal of Hepatology》报道,中国肝病患者人数规模已经约有4亿人,其中NAFLD患者人数最多,高达1.73亿至3.1亿人。另据公开数据表示,普通成人NAFLD患病率约为10%~30%,其中10%~20%为非酒精性脂肪性肝炎(Non-alcoholic steatohepatitis,NASH),后者在10年内发展为肝硬化的几率高达25%[2]。
NAFLD的发生首先会对肝脏造成损害,如果不能早发现以及早干预,严重则会发展为肝硬化,乃至肝癌。研究也进一步显示NAFLD与代谢综合征(Metabolic syndrome,Mets)、2型糖尿病(Type 2 diabetes mellitus,T2DM)、慢性肾脏疾病(Chronic kidney disease,CKD),甚至肝内肿瘤等高发密切相关[3-5]。
由于肝脏没有痛感神经,NAFLD人群在初期阶段一般没有明显症状,因此容易被消费者所忽视,也被称为健康的“隐形杀手”。
2. 远离NAFLD,拒绝“肝”扰
那么NAFLD到底如何发生的?排除饮酒和其他明确的肝损害因素外,例如不良饮食习惯—高热量、高脂肪、高糖分的饮食,最终导致肝细胞内脂肪过度沉积,进而形成获得性代谢应激肝损伤。
一般而言,正常人肝组织中会含有少量的脂肪,肝脏功能受损就与肝内脂肪的堆积直接相关。目前肝脏内脂肪形成主要有3个来源,包含三餐摄入的脂肪;肝脏储存的脂肪;脂肪酸通过血液到达肝脏,进一步合成脂肪(占比达65%)。
其中脂肪酸积累会引起肝脏脂肪变性(Hepatic steatosis),当脂肪形成超过消耗时,就会出现肝细胞损伤。受损的肝细胞会分泌更多炎症因子,进一步诱发更严重的、不可逆的肝疾病,如肝纤维化、肝硬化和肝癌等[6]。
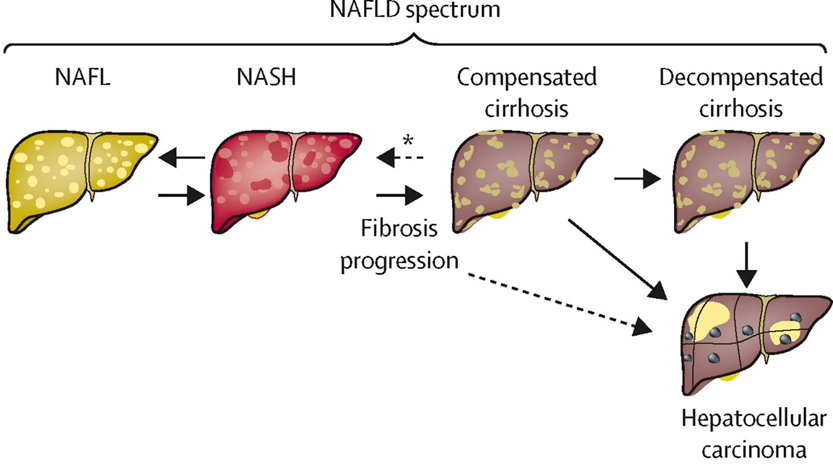
图示:脂肪肝损伤发病进程
在新时代下,人们对于肝脏健康的保护提出了新要求。想要提升护肝战斗力,不仅要重视肝细胞脂质代谢,同时要及时改善肝损伤,做好保护和修复,岩藻黄素就为缓解NAFLD的研究提供一条新途径。
3. 岩藻黄素:由内守护,为肝减负
岩藻黄素是一种脂溶性色素,存在于藻类中的一种天然类胡萝卜素含氧衍生物,也是自然界丰度最高的类胡萝卜素分子之一。其结构中含有一个异位键、一个共轭羰基、一个5,6-单环氧化物和一个乙酰基,对细胞膜和组织有较好的穿透性。
近年来有多项临床实验表明,其在新陈代谢、炎症反应、紫外线损伤、氧化应激、神经养护、肝脏健康、血糖血脂、体重管理等方面均有积极作用。这其中,尤以非酒精性脂肪肝方面的研究最为突出[7-10]。
《Diabetes Obesity And Metabolism》发布的一项临床研究证实,岩藻黄素可以改善NAFLD患者的肝脏脂肪含量、血清甘油三酯和炎症因子水平和肝功能指标[11];《Marine Drugs》的临床试验也证实岩藻黄素可以显著缓解NAFLD患者的肝脂肪沉积,进而提高肝功能[7]。

图示:岩藻黄素可以改善NAFLD的临床研究
另外研究进一步证实了岩藻黄素对NAFLD患者肝损伤的改善作用及其潜在机制,如降低肝脏脂肪酸毒性、抑制肝脏脂肪变性和肝脏纤维化等[7]。那么岩藻黄素是如何对NAFLD产生积极影响的呢?
一方面,岩藻黄素可通过一系列细胞因子激活白色脂肪组织中线粒体解偶联蛋白UCP1的表达,加速脂肪分解;同时抑制脂肪酸合成酶FAS的mRNA水平,来降低脂肪合成;还可通过降低胰岛素受体底物IRS-1的磷酸化,抑制葡萄糖在成熟脂肪细胞中的吸收。
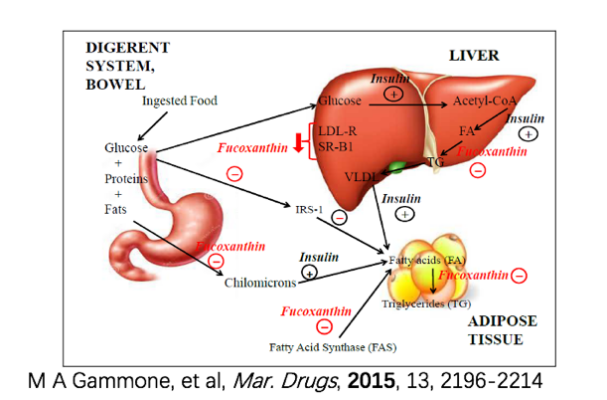
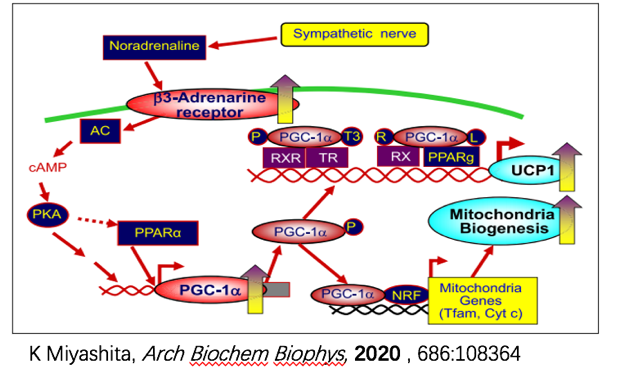
另外一方面,岩藻黄素可下调低密度脂蛋白受体LDL-R和清道夫受体SR-B1减少甘油三酯和胆固醇在血液和肝脏中的吸收;并通过对胆固醇调节酶活性的正向影响以及对脂质代谢相关基因表达的影响,显著降低血液和肝脏中的甘油三酯浓度。
4. FucoRuby™岩藻黄素:为“肝脏健康”提供专业守护
相较于其他大型褐藻,微藻是岩藻黄素的最佳来源。德默特作为全球微藻基产品供应商,通过高通量筛选技术,从上万种藻类中挑选出具有经济特性、高目标含量的藻种,例如选择单细胞硅藻,作为提取高纯度的岩藻黄素(FucoRuby™)的目标藻种。

当“养肝护肝”的产品成为市场关注焦点,FucoRuby™岩藻黄素作为一款天然的海洋功能性成分,德默特对产品及其功能活性成分进行了确证研究。采用FucoRuby™岩藻黄素进行的动物实验表明,其有助于改善高脂诱导的肝脏损伤,如降低肝细胞的氧化应激水平、缓解肝组织的炎症、减少肝组织的纤维化以及减轻肝脏凋亡水平;还可通过促进蛋白质和肝糖原的合成、降低脂肪和胆固醇的合成来改变肝组织的碳流分配。多重实验证实对于非酒精性脂肪肝具有积极的保护作用,并且试验过程中岩藻黄素对大鼠没有产生不良影响。
在生产环节,企业意识到传统培养微藻生产方式下容易出现环境条件不可控,产品品质不稳定等系列问题。为了更好地造福消费者,实现FucoRuby™岩藻黄素的商业化应用,德默特借助 “光碳智造”技术,给目标藻种精准调控藻类培养所需的最适光谱与碳谱,大幅度提升微藻培养的光能转换效率,满足全天候、全周期的藻类稳定生产,为未来终端产品应用的创新突破性发展注入新的活力。
在未来,德默特将持续不断地对微藻进行投入和研发,面向全球输出高品质的岩藻黄素原料和应用解决方案,以更好的满足当今消费者的升级诉求,为“肝脏健康”提供专业守护。
参考文献
[1]天猫健康《2023健康年度词》
[2]《非酒精性脂肪性肝病防治指南》
[3]Younossi, Z., et al., Global burden of NAFLD and NASH: trends, predictions, risk factors and prevention. Nat Rev Gastroenterol Hepatol, 2018. 15(1): p. 11-20.
[4]Adams, L.A., et al., Non-alcoholic fatty liver disease and its relationship with cardiovascular disease and other extrahepatic diseases. Gut, 2017. 66(6): p. 1138-1153.
[5]Anstee, Q.M., G. Targher, and C.P. Day, Progression of NAFLD to diabetes mellitus, cardiovascular disease or cirrhosis. Nat Rev Gastroenterol Hepatol, 2013. 10(6): p. 330-44.
[6]Hou, X.J., et al., Immune response involved in liver damage and the activation of hepatic progenitor cells during liver tumorigenesis. Cell Immunol, 2018. 326: p. 52-59.
[7]Shih, P.H., et al., Fucoidan and Fucoxanthin Attenuate Hepatic Steatosis and Inflammation of NAFLD through Modulation of Leptin/Adiponectin Axis. Mar Drugs, 2021. 19(3).
[8]Guo, B., et al., Lipid-Lowering Bioactivity of Microalga Nitzschia laevis Extract Containing Fucoxanthin in Murine Model and Carcinomic Hepatocytes. Pharmaceuticals (Basel), 2021. 14(10).
[9]Takatani, N., et al., Fucoxanthin inhibits hepatic oxidative stress, inflammation, and fibrosis in diet-induced nonalcoholic steatohepatitis model mice. Biochem Biophys Res Commun, 2020. 528(2): p. 305-310.
[10]Ye, J., et al., Fucoxanthin Attenuates Free Fatty Acid-Induced Nonalcoholic Fatty Liver Disease by Regulating Lipid Metabolism/Oxidative Stress/Inflammation via the AMPK/Nrf2/TLR4 Signaling Pathway. Mar Drugs, 2022. 20(4).
[11]Abidov, M., et al., The effects of Xanthigen in the weight management of obese premenopausal women with non-alcoholic fatty liver disease and normal liver fat. Diabetes Obes Metab, 2010. 12(1): p. 72-81.
>>>声明
*新营养(xinyingyang.com)致力于秉承循征营养学的理念,重度垂直人类营养,为广大健康原辅料供应商和消费者之间架起沟通的桥梁,标明原创的文章权限为本网所有,如需转载请得到书面申请并在文章开头注明出处。
*文章中会充列示参考文献,但因商业利益相关造成的不客观可能依然存在,欢迎读者多提出批评意见和建议。
*文章中涉及功效相关描述均有对应的数据支持,囿于篇幅限制无法全部刊登,如需数据来源,可向新营养(xinyingyang.com)或文章中涉及到的企业索取。文章图片部分来源于网络,如有侵权请告知删除。
*此公众号中全部内容仅为一般性参考。读者不应在缺乏具体的专业建议的情况下,擅自根据文章内容中的任何信息采取行动。此公众号运营方将不对任何因采用文章内容而导致的损失负责。
*文章中涉及的产品、成分、功效仅代表相关企业的观点,新营养仅基于信息传递目的进行转述,并不代表我们绝对认同相关宣称,也不支持任何产品的营销和销售。
*文章中插入的图片不涉及到商业行为,仅限交流,并标明了来源出处,尊重原创图片设计。
新营养留言互动
您的电话不会被公开。 必填项已用 * 标注
相关热词搜索:
上一篇:聚焦新品 | 多维度解读益生菌口腔健康概念新品BLIS® by Probi普诺碧®
下一篇:摆脱痛风困扰,Cell子刊揭示肠道菌群与高尿酸血症的研究新成果
新营养峰会/活动
新营养热门资讯
共晶技术:让营养素步入埃米时代
XINGRAPHIC · 09-11
11月6-7日广州新营养趋势大会!30+演讲、2
风信社 · 09-08
当“造物”成为可能,人类营养健康产业将迎
XINGRAPHIC · 07-07
新营养周报 | 农夫山泉上新蓝靛果混合汁
数据 / 观察 · 01-06