特殊人群资讯
干酪乳酪杆菌IOB-P9燕麦后生元对高脂饮食诱导肥胖大鼠体脂代谢及肝功能支持的研究
2025-12-05 09:28 来源:新营养
文/创源生物
 图源:摄图网
图源:摄图网
当下秋冬养生市场普遍围绕“进补”展开,但传统的高脂“贴秋膘”习惯,加上活动量减少,暗藏健康隐患。
研究显示,我国秋冬季节成人高脂饮食摄入及代谢问题风险呈季节性升高趋势:针对男性群体的跨季节膳食追踪研究显示,冬季饱和脂肪、膳食胆固醇摄入量显著高于夏季,且与体重指数(BMI)、血清总胆固醇及低密度脂蛋白胆固醇(LDL-C)升高呈正相关[1];上海市2012-2014 年居民膳食调查及闵行区四季膳食质量评估均证实,冬季红肉、畜禽肉等动物性食物摄入达四季峰值,膳食失衡程度最严重,脂肪供能比达37.99%,显著高于夏季,这一饮食变化推动肥胖及代谢问题风险攀升[2]。
同时,肝脏作为脂质代谢的核心器官首当其冲,脂肪过度沉积可引发非酒精性脂肪肝。根据国内流行病学调查,我国超30%的成人因长期高脂饮食存在不同程度的肝脏脂质沉积,其中肥胖人群的非酒精性脂肪肝患病率更是高达60%以上[3],这些问题不仅影响肝脏功能,还会反过来加重全身代谢紊乱,形成“代谢-肝脏”双重损伤的恶性循环。
在全球肥胖及相关代谢问题发病率持续攀升的大背景与 “健康中国 2030” 战略的双重驱动下,通过对传统营养食品原料进行现代化改造,从而实现 “代谢调节 + 器官保护” 的双重功效,目前已成为当前营养健康领域的研究热点。
天津市食用益生菌重点实验室最新的研究结果证实,天津创源生物明星原料——干酪乳酪杆菌IOB-P9燕麦后生元通过“精智固态发酵技术赋能+后生元特性加持”的创新模式,可正向影响高脂饮食诱导肥胖大鼠的体脂代谢紊乱,并修复受损肝功能,为肥胖相关代谢问题的膳食干预提供了坚实的循证依据与创新方向[4]。
01
肥胖干预的核心痛点
与燕麦后生元的技术突破
传统燕麦的局限
传统燕麦产品主要依靠膳食纤维的物理饱腹感辅助体重管理,但其作用机制相对单一,难以针对脂肪合成与分解的关键代谢通路进行主动调节。此外,燕麦中天然存在的大分子β-葡聚糖由于结构特性,其实际生物利用度有限。研究表明,大分子β-葡聚糖在人体中的吸收率通常低于30%[5],因此对于已形成的肥胖及相关代谢异常,如肝脏脂质沉积等,传统燕麦产品的健康作用较为有限。
后生元的技术创新
精智固态发酵技术是创源生物基于自主筛选的优良功能菌株,结合智能化固态发酵设备,以药食同源物质为基质,采用具有自主知识产权的分段固态发酵复配技术实现多菌种协同增效,进而制备富含多种生物活性成分的新型药食同源后生元制剂。该技术通过多菌株协同、精细化参数调控与智能化过程控制的固态发酵方式,并结合肠道仿生技术,能保留更多发酵活性精华,使产生的益生菌体、代谢产物和发酵营养物被完全保留,促进产品协同增效,达成产物活性成分与底物功能效果的双重提升;同时,采用特定灭活工艺可消除菌体繁殖能力,又能完整保留其微生物结构、特性及功能活性,进一步增强产品的稳定性和生物利用度;此外,独有的绿色低碳工艺还能降本增效、实现环境友好。
干酪乳酪杆菌IOB-P9燕麦后生元通过精智固态发酵技术,深度融合燕麦与干酪乳酪杆菌IOB-P9的优势——既保留燕麦膳食纤维的基础作用,又通过发酵生成灭活菌体及其代谢产物。
02
动物试验验证对体脂代谢的精准调控:
从“减重”到“减脂”的本质突破
研究团队通过连续10周灌胃干预高脂饮食诱导的肥胖大鼠(分为空白对照组、模型组、低/高剂量后生元组),结果证实IOB-P9燕麦后生元可从“体脂分布、血脂水平”双维度影响大鼠的代谢紊乱。
在高脂肥胖大鼠干预实验中,IOB-P9燕麦后生元可改善大鼠的体脂分布、调节血脂与血糖水平:能针对性减少内脏脂肪堆积,缓解血脂紊乱,同时稳定空腹血糖[3]。该结果的核心意义在于,它突破了传统燕麦“只饱腹、不减脂”的局限——不再是单纯依赖减少进食量的“被动减重”,而是通过调节体脂代谢通路,实现“减脂肪、稳代谢”的健康减重目标,为解决肥胖人群“吃少仍胖”的代谢难题提供了新思路。
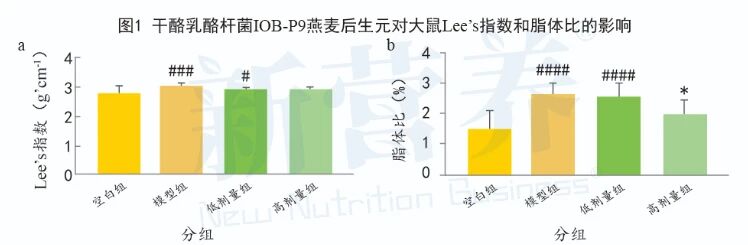 图1 干酪乳酪杆菌IOB-P9燕麦后生元对大鼠Lee’s 指数和脂体比的影响
图1 干酪乳酪杆菌IOB-P9燕麦后生元对大鼠Lee’s 指数和脂体比的影响
03
动物试验验证对肥胖相关激素紊乱的调节:从“代谢失衡”到“信号修复”
肥胖常伴随激素调节失控,尤其是瘦素(LEP)抵抗与皮质酮(CORT)过度分泌,二者形成“食欲亢进-脂肪堆积”的恶性循环,进一步加剧肥胖。
瘦素由脂肪组织分泌,其血清水平与体脂量正相关,肥胖状态下易出现“瘦素抵抗”,即瘦素血清水平升高却无法有效抑制食欲。皮质酮是促进食欲与脂肪堆积的糖皮质激素,长期慢性升高会显著加剧肥胖程度。
经动物试验验证可得,IOB-P9燕麦后生元可通过靶向调节大鼠的这两种激素,打破恶性循环。其核心机制可能与后生元诱导肠道菌群产生短链脂肪酸(乙酸、丙酸)相关:短链脂肪酸可激活肠道FFAR2 受体,抑制促炎因子(如脂多糖)入血,进而下调皮质酮合成,并改善瘦素受体表达,恢复激素信号的正常调节功能[6,7]。
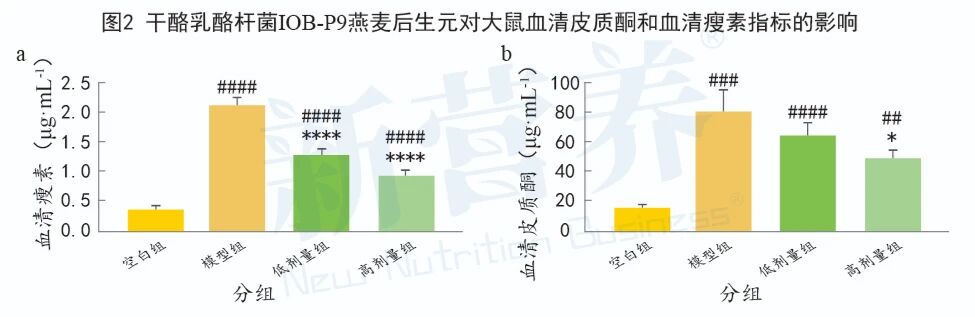 图2 干酪乳酪杆菌IOB-P9燕麦后生元对大鼠血清皮质酮和血清瘦素指标的影响
图2 干酪乳酪杆菌IOB-P9燕麦后生元对大鼠血清皮质酮和血清瘦素指标的影响
04
动物试验验证对受损肝功能的修复:
从“指标改善”到“组织修复”
肝脏是脂质代谢的核心器官,高脂饮食引发的肥胖常导致肝细胞脂肪变性(非酒精性脂肪肝),表现为肝功能指标异常与组织形态损伤。经动物试验验证可得,IOB-P9燕麦后生元可通过“指标调节+组织修复”双重路径保护大鼠肝脏。
这一过程可能与IOB-P9燕麦后生元激活大鼠肝脏AMPK通路相关:AMPK是“代谢总开关”,其激活后可发挥三重作用:一是促进脂肪分解相关蛋白(如PPARα,过氧化物酶体增殖物激活受体α)的表达;二是抑制脂肪合成基因(如SREBP-1C)的活性;三是减少肝细胞氧化应激损伤,最终实现肝功能修复与肝组织保护[8]。
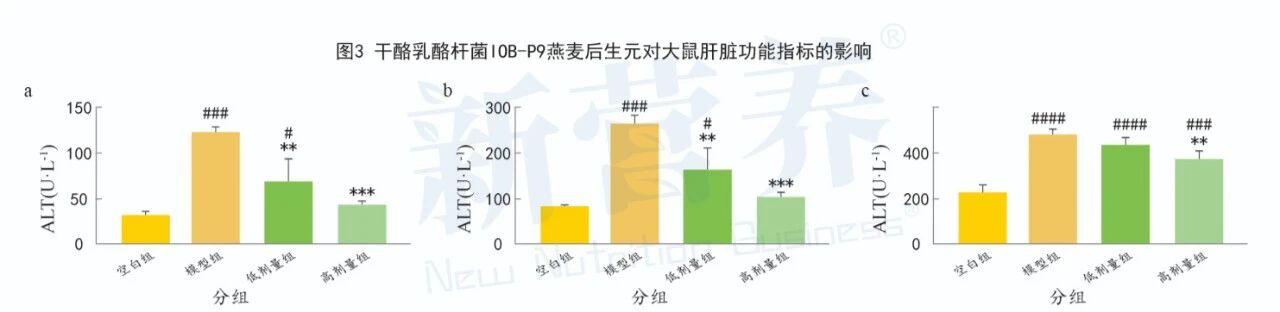 图3 干酪乳酪杆菌IOB-P9燕麦后生元对大鼠肝脏功能指标的影响
图3 干酪乳酪杆菌IOB-P9燕麦后生元对大鼠肝脏功能指标的影响
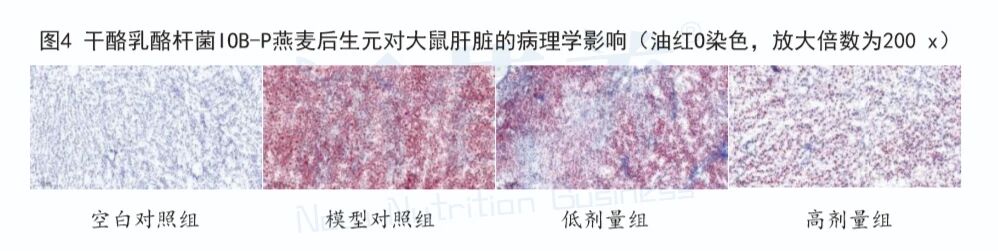 图4 干酪乳酪杆菌IOB-P9燕麦后生元对大鼠肝脏的病理学影响(油红O染色,放大倍数为200 x)
图4 干酪乳酪杆菌IOB-P9燕麦后生元对大鼠肝脏的病理学影响(油红O染色,放大倍数为200 x)
05
结语:从实验室到功能性食品的转化价值
干酪乳酪杆菌IOB-P9燕麦后生元的相关研究,是功能性膳食干预领域的重要突破——该研究通过严格的动物实验(以高脂饮食诱导的肥胖大鼠为模型),证实了“燕麦基质+特定益生菌定向发酵”形成的后生元体系,在调控体脂代谢与保护肝功能方面存在协同效应。
这一研究的价值不仅限于基础科研领域,其丰富且严谨的科学循证数据(涵盖代谢指标、分子机制、组织病理等多维度验证),为功能性食品的产业化开发奠定了扎实理论基础。该研究由创源生物主导推进,作为在固态发酵后生元原料领域深耕的企业,创源生物凭借其自主研发的多种益生菌分段固态发酵技术,实现了从实验室研究到产业化应用的高效转化。在干酪乳酪杆菌IOB-P9 燕麦后生元的开发中,企业依据菌株特性,通过精准控制的发酵工艺,在燕麦基质中实现了活性成分的高效富集与转化,为后生元的多元化产品开发提供了可靠的技术支撑。
未来,可围绕肥胖人群的不同消费场景与需求,设计多元化产品形态:针对日常饮品场景,开发低热量、高纤维的发酵燕麦饮,通过优化发酵工艺保留后生元活性成分,兼顾适口性与功能性;针对代餐需求,研发富含优质蛋白与复合碳水的发酵燕麦代餐粉,搭配维生素、矿物质等微量营养素;甚至可拓展至烘焙食品、即食麦片等品类,让功能性干预融入日常膳食。
更重要的是,该研究推动了“以食代疗”肥胖干预理念的落地实践——相较于药物干预可能存在的副作用(如胃肠道不适、肝肾功能负担),发酵燕麦后生元基于天然食材与益生菌发酵,具有安全性高、耐受性好、易长期坚持的优势。随着后续人体临床试验的推进与产品技术的迭代,这类功能性食品有望成为大众健康领域的“轻干预”新选择,也为食品行业从“营养供给”向“健康干预”转型提供了可复制的研发范式,助力推动全民健康膳食体系的完善。
参考文献
[1] Pieterse M, Kruger H S, Groenewald P J. Seasonal cycles in food purchases and changes in BMI among South Africans participating in a health promotion programme[J]. Public Health Nutrition, 2016, 19(17): 3174-3182.
[2] 上海市疾病预防控制中心。上海市2012—2014 年居民膳食营养状况及季节特征研究[J]. 营养学报, 2025, 47 (2): 145-150.
[3]《中国脂肪肝防治指南(科普版)》[J].中国出版,2015,(06):73.DOI:CNKI:SUN:ZGCB.0.2015- 06-021.
[4] 赵范,孙韵琪,闫梦娜,等。干酪乳酪杆菌IOB-P9 燕麦后生元对高脂饮食诱导肥胖大鼠体脂代谢及肝功能的改善效应[J].现代食品科技,2026 (已录用待正式发表).
[5]El Khoury, D., Cuda, C., Luhovyy, B. L., Anderson, G. H., Beta Glucan: Health Benefits in Obesity and Metabolic Syndrome, Journal of Nutritionand Metabolism, 2012, 851362, 28 pages, 2012. https://doi.org/10.1155/2012/851362
[6]肖灵,唐琳琳,宋晓妍,等.后生元调节肠道微生态及减少脑内β-淀粉样蛋白沉积改善阿尔茨海默病大鼠的认知障碍[J].食品科学,2025,46(5):182-193.
[7] LI S, LIU M, CAO S, et al. The Mechanism of the Gut-Brain Axis in Regulating Food Intake[J]. Nutrients, 2023, 15(17): 3728.
[8] ZHONG Y, WANG T, LUO R, et al. Recent advances and potentiality of postbiotics in the food industry: Composition, inactivation methods, current applications in metabolic syndrome, and future trends[J]. Crit Rev Food Sci Nutr, 2024, 64(17): 5768-5792.
END
>>>声明
*新营养(xinyingyang.com)致力于秉承循征营养学的理念,重度垂直人类营养,为营养健康产业从业者架起沟通的桥梁,标明原创的文章权限为本网所有,如需转载请得到书面申请并在文章开头注明出处。
*文章中会充列示参考文献,但因商业利益相关造成的不客观可能依然存在,欢迎读者多提出批评意见和建议。
*文章中涉及功效信息内容均有对应的数据支持,囿于篇幅限制无法全部刊登,如需数据来源,可向新营养(xinyingyang.com)或文章中涉及到的企业索取。文章图片部分来源于网络,如有侵权请告知删除。
*此公众号中全部内容仅为创新案例的一般性参考。读者不应在缺乏具体的专业建议的情况下,擅自根据文章内容中的任何信息采取行动。此公众号运营方将不对任何因采用文章内容而导致的损失负责。
*文章中涉及的产品、成分、功效仅代表相关企业的观点,新营养仅基于信息传递目的进行转述,并不代表我们绝对认同相关宣称,也不支持任何产品的营销和销售。
*文章中插入的图片不涉及到商业行为,仅限交流,并标明了来源出处,尊重原创图片设计。
新营养留言互动
您的电话不会被公开。 必填项已用 * 标注
相关热词搜索:
上一篇:黑升麻、染料木素......热门女性补剂深度分析,S-雌马酚如何强势突围?
下一篇:体重管理“黑科技”——薇安生物带您探秘辣椒素背后的科学
新营养峰会/活动
新营养热门资讯
共晶技术:让营养素步入埃米时代
XINGRAPHIC · 09-11
11月6-7日广州新营养趋势大会!30+演讲、2
风信社 · 09-08
当“造物”成为可能,人类营养健康产业将迎
XINGRAPHIC · 07-07
新营养周报 | 农夫山泉上新蓝靛果混合汁
数据 / 观察 · 01-06