法规资讯
重磅利好「食药物质」及「营养产业」!深入分析背景、优势与行业影响!海关总署等四部门关于试点实施进口食药物质分类管理措施的
2025-12-23 17:13 来源:新营养
 图源:摄图网
图源:摄图网
一、法规背景
2025年12月4日,海关总署、国家卫生健康委、市场监管总局、国家药监局联合发布《关于试点实施进口食药物质分类管理措施的公告》(以下简称《公告》),对部分食药物质的进口管理进行试点改革。这一政策的出台,与当前中国食品与药品进口监管体系的复杂性密切相关。
 在传统监管模式下,进口食药物质(如中药材、药食同源原料等)往往面临“一刀切”的审批要求。
在传统监管模式下,进口食药物质(如中药材、药食同源原料等)往往面临“一刀切”的审批要求。
例如,《进口药材管理办法》明确要求首次进口药材需取得国家药监局核发的《进口药材批件》,并经口岸检验合格后方可通关;
而《药品进口管理办法》则规定进口药品需凭《进口药品注册证》或《进口药品批件》办理通关手续,且麻醉药品、精神药品等特殊品类需额外提交《进口准许证》。
这种模式虽然保障了药品质量安全,但对部分“食药物质”或“药食同源”物质(既可作为食品原料,也可作为药品使用)的进口流程造成了一定负担。
例如,若企业进口某食药物质用于食品加工而非药品用途,仍需提交《进口药品通关单》,导致通关效率降低、成本增加。
《公告》的试点改革,正是针对这一痛点。其核心背景包括:
·优化口岸营商环境:近年来,中国持续推动贸易便利化改革,简化通关流程、降低合规成本是重要目标。此次试点通过分类管理,减少非必要审批环节,直接回应企业诉求[1]。
·支持食药物质进口贸易发展:食药物质作为食品与药品产业的重要原料,其进口需求与日俱增。但传统监管模式因分类模糊,可能阻碍企业快速获取原料,影响产业发展。试点通过清单化管理,明确“药用”与“非药用”用途的区分标准,为贸易提供确定性[1]。
·回应行业多元化需求:随着大健康产业发展,食药物质的应用场景从传统药品扩展至保健食品、特医食品、普通食品等领域。此前的监管体系未能充分适应这种多元化需求,《公告》通过分类管理,更精准地匹配不同用途的监管要求[1]。
 二、法规优势分析
二、法规优势分析
《公告》的试点改革在监管效率、合规便利性和产业适配性方面具有显著优势,主要体现在以
四点:
1.简化通关流程,降低企业成本
《公告》明确,对《试点实施进口分类监管食药物质清单》中的商品,若进口申报为“药用用途”,仍需提交《进口药品通关单》;但若申报为“其他用途”(如食品原料),则免于提交《进口药品通关单》[1]。这一调整直接减少了非药用场景的通关环节,避免企业因重复提交文件而产生的行政成本与时间成本。例如,某企业进口用于保健食品的枸杞,若此前需按药品标准提交通关单,流程可能涉及省级药监部门审批、口岸检验等多环节;而试点后,若申报用途为食品原料,则可直接办理通关,无需等待药监部门的审批结果。
2.清单化管理提升政策透明度与可操作性
试点通过动态更新的清单(《试点实施进口分类监管食药物质清单》)明确适用范围,企业可直接查询清单中的物质及其用途分类[1]。这种透明化管理降低了政策执行的不确定性,企业无需通过模糊的法规条文自行判断适用性,而是以清单为准,减少因误判用途导致的合规风险。
3.强化部门协同监管,保障质量安全
《公告》要求海关总署、市场监管总局和国家药监局在各自职责范围内,对进口食药物质的进口、经营、加工等环节加强监管,并建立食品安全国家标准与监管信息的共享机制[1]。这一优势在于:
·跨部门协作:传统监管中,食品与药品的审批、检验、备案等环节由不同部门负责,可能存在信息孤岛。试点后,四部门通过信息共享机制(如药典标准、口岸检验数据),可更高效协调监管资源,避免重复检验或审批。
·精准定位风险:针对“药用用途”仍需严格检验,而“其他用途”则以食品标准管理,监管部门可更聚焦于高风险场景(如药品),降低对低风险场景(如食品原料)的干预,提升整体监管效能。
4.动态调整机制适应产业变化
《公告》强调清单将“动态更新”,并允许企业通过合法途径调整用途申报[1]。这一机制的优势在于:
·灵活性:食药物质的用途可能随市场或技术进步而变化(如某物质从药用转向食品添加剂),动态清单可及时反映这些变化,避免因政策滞后导致企业被动调整。
·鼓励创新:试点允许企业在合规前提下探索新用途(如将部分药材用于功能性食品),为行业创新提供政策空间,同时通过监管确保安全。
三、对食药物质行业的指导意义
食药物质行业涵盖中药材、药食同源原料、功能性食品原料等,其进口管理直接影响行业供应链稳定性与合规成本。《公告》的试点改革对行业的指导意义主要体现在以下三方面:
1.明确用途分类,规范企业行为
《公告》要求企业在办理进口通关手续时,明确申报产品用途,并承担“依法如实申报责任”[1]。这一规定从源头上规范了企业的经营行为:
·防止用途混淆:此前,部分企业可能通过模糊申报或虚假用途规避监管,导致药用物质被非法流入食品市场,或食品原料被违规用于药品生产。试点后,企业需严格区分用途,申报不实将面临法律责任(如查封扣押、行政处罚)[1]。
·强化主体责任:企业需建立内部合规体系,确保申报用途与实际用途一致。例如,进口用于保健食品的食药物质需在合同、生产计划中明确标注用途,避免因后续用途变更而违反法规。
2.促进贸易便利化,稳定供应链
对于非药用用途的食药物质,免于提交《进口药品通关单》的政策直接缩短了通关时间[1]。以进口用于普通食品的食药物质为例,此前需等待药监部门审批通关单(通常需20-30日),流程复杂;试点后,企业仅需按食品进口要求提交文件,通关效率大幅提升。这对依赖进口原料的食品加工企业(如中药饮品、功能性食品企业)至关重要,有助于稳定供应链、降低库存成本。
3.推动产业升级与合规化发展
试点通过清单化管理和动态更新,引导企业聚焦合规、高质量的食药物质进口。例如,清单中可能优先纳入符合中国药典或食品标准的物质,淘汰不符合质量要求的品类。同时,监管部门对药用用途的严格检验(如需提交《进口药品注册证》或《进口药品批件》),倒逼企业提升原料质量,推动行业从“粗放式”进口向“高标准、合规化”转型。此外,信息共享机制(如监管部门共享检验数据、标准信息)有助于企业获取最新监管动态,避免因信息滞后导致的合规风险[1]。
四、对营养产业的影响
营养产业(如保健食品、特医食品、功能性食品)是食药物质进口的重要下游领域。《公告》的试点改革对营养产业的影响可从以下两方面分析:
1.原料供应的便捷性与成本优化
试点后,用于食品或保健食品的食药物质进口流程简化,企业无需再提交《进口药品通关单》[1]。这一政策直接影响营养产业的原料成本与供应效率:
·降低通关成本:此前,进口非药用食药物质需支付通关单审批费用,流程耗时较长;试点后,企业仅需按食品进口要求办理,节省了时间与经济成本。
·提升供应链稳定性:对于依赖进口原料的营养企业,试点政策减少了通关环节的不确定性,企业可更精准规划生产计划,避免因审批延迟导致的原料短缺。
2.合规风险与质量要求的双重挑战
尽管试点简化了部分流程,但对用途申报的真实性提出了更高要求。若企业进口食药物质用于食品,但实际用于药品或未申报用途,将面临监管部门的查封、扣押及行政处罚[1]。这对营养产业的影响包括:
·合规压力增加:企业需建立完善的用途申报与追溯体系,确保进口文件(如合同、用途声明)与实际生产用途一致。例如,某企业进口用于保健食品的灵芝孢子粉,需在进口报关单中明确标注“食品原料”,并留存相关证明文件。
·质量要求趋严:非药用用途的食药物质虽免于提交通关单,但仍需符合食品标准(如《食品安全法》及其实施条例)。监管部门可能通过抽查或信息共享机制(如与药监局、市场监管局协同)加强事后监管,倒逼企业提升原料质量。
五、中国与外资企业的布局建议
《公告》的试点改革对企业的进口策略、合规管理及市场拓展提出了新的要求。针对中国企业和外资企业,建议从以下方向布局:
1.中国企业的应对策略
·精准申报用途:企业需在进口前明确食药物质的实际用途,并据此选择通关路径。例如,若进口用于普通食品,应避免按药用用途申报,以节省通关成本;若用于药品,则需提前准备《进口药品注册证》《通关单》等文件[1]。
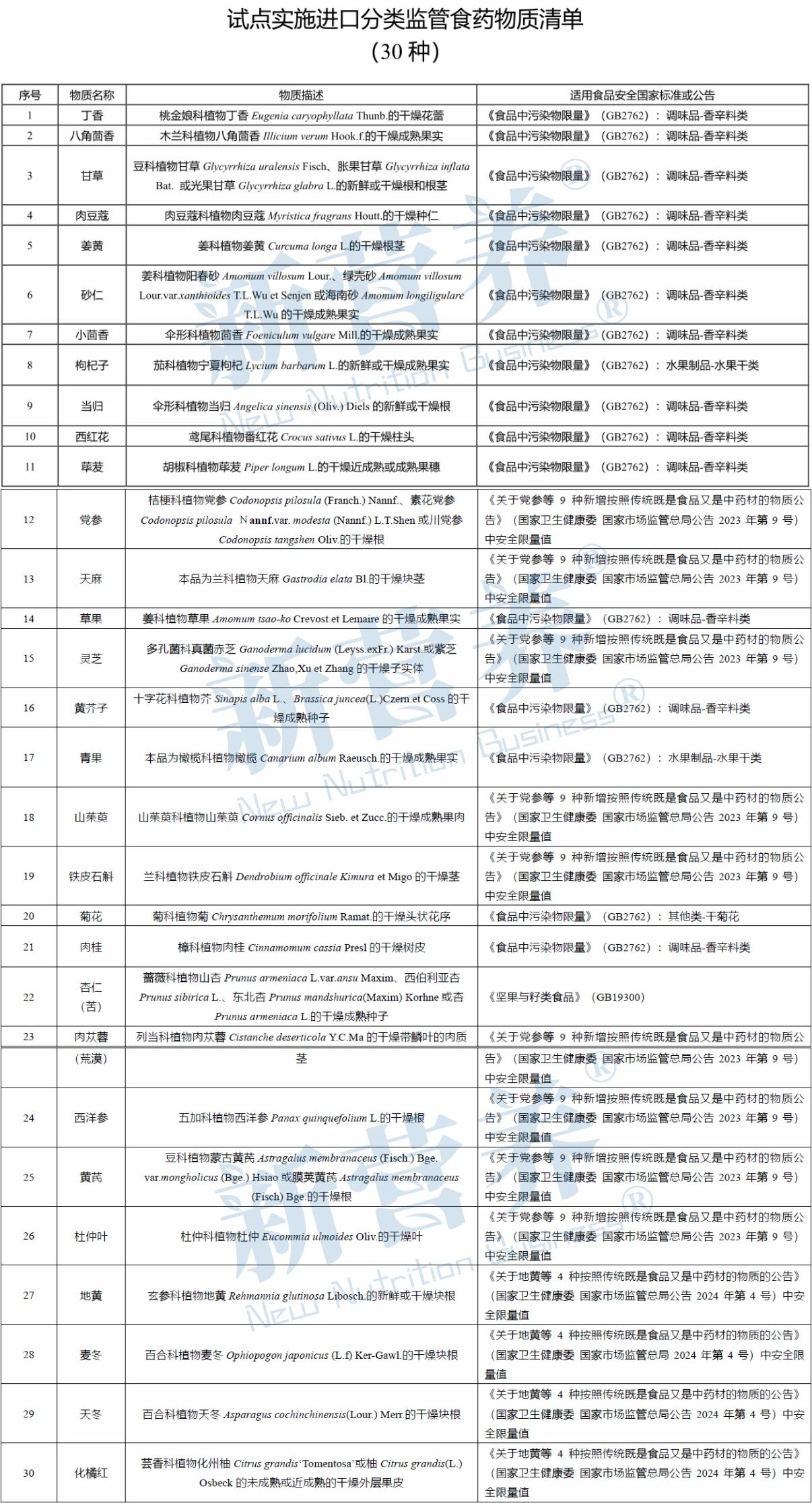
·动态跟踪清单更新:试点清单将动态调整,企业需定期查询《试点实施进口分类监管食药物质清单》(附件),及时了解新增或调整的物质及其用途分类。例如,若某物质从药用用途调整为食品用途,企业可优化供应链,降低合规成本。
·加强内部合规体系:企业需建立从采购、通关到加工的全流程合规管理,确保申报用途与实际用途一致。例如,设立专门的合规部门,审核进口合同中的用途条款,并留存相关记录以备监管检查[1]。
2.外资企业的应对策略
·适应中国监管逻辑:外资企业需理解中国对“药用”与“非药用”用途的严格区分,并据此调整出口策略。例如,若出口物质用于中国食品产业,需确保其符合《食品安全法》要求,并避免因用途混淆导致的通关延误。
·与国内进口商合作:外资企业可通过与具备资质的国内进口商合作,确保进口申报的合规性。例如,国内进口商需持有《药品生产许可证》《药品经营许可证》等资质(如《药品进口管理办法》要求),外资企业可提前筛选合作方,避免因资质问题导致的通关失败。
·关注清单扩展可能性:试点清单可能逐步扩展至更多食药物质,外资企业可积极与监管部门沟通,推动其出口物质纳入清单,并明确用途分类。例如,若某外资企业出口的食药物质此前因用途模糊被限制,可通过提供用途证明(如合同、生产标准)争取纳入清单。
六、结论与展望
《关于试点实施进口食药物质分类管理措施的公告》是中国在食品与药品进口监管领域的创新尝试,其核心在于通过清单化管理、用途分类和部门协同,优化营商环境、降低合规成本,同时保障质量安全。这一政策对食药物质行业和营养产业的影响深远:前者需规范用途申报并提升供应链效率,后者则可享受原料进口便利,但也面临更严格的合规与质量要求。
未来,随着试点经验的积累,清单范围可能进一步扩大,更多食药物质将纳入分类管理。同时,监管部门可能通过信息共享机制(如与海关、药监局、卫健委的联动)强化事后监管,确保企业不滥用“其他用途”豁免。企业需密切关注政策动态,提前布局合规体系,以在竞争中占据优势。
参考文献:
[1]海关总署等四部门发布关于试点实施进口食药物质分类管理措施的公告(2025年12月4日)
END
>>>声明
**竞合岛®致力于秉承循征营养学的理念,重度垂直人类营养,为营养健康产业从业者架起沟通的桥梁,标明原创的文章权限为本网所有,如需转载请得到书面申请并在文章开头注明出处。
*文章中会充列示参考文献,但因商业利益相关造成的不客观可能依然存在,欢迎读者多提出批评意见和建议。
*文章中涉及功效信息内容均有对应的数据支持,囿于篇幅限制无法全部刊登,如需数据来源,可向竞合岛®或文章中涉及到的企业索取。文章图片部分来源于网络,如有侵权请告知删除。
*此公众号中全部内容仅为创新案例的一般性参考。读者不应在缺乏具体的专业建议的情况下,擅自根据文章内容中的任何信息采取行动。此公众号运营方将不对任何因采用文章内容而导致的损失负责。
*文章中涉及的产品、成分、功效仅代表相关企业的观点,新营养仅基于信息传递目的进行转述,并不代表我们绝对认同相关宣称,也不支持任何产品的营销和销售。
*文章中插入的图片不涉及到商业行为,仅限交流,并标明了来源出处,尊重原创图片设计。
新营养留言互动
您的电话不会被公开。 必填项已用 * 标注
相关热词搜索:
上一篇:市场监管总局就《广告引证内容执法指南(征求意见稿)》公开征求意见
下一篇:市场监管总局食品安全专题新闻发布会实录
新营养峰会/活动
新营养热门资讯
共晶技术:让营养素步入埃米时代
XINGRAPHIC · 09-11
11月6-7日广州新营养趋势大会!30+演讲、2
风信社 · 09-08
当“造物”成为可能,人类营养健康产业将迎
XINGRAPHIC · 07-07
新营养周报 | 农夫山泉上新蓝靛果混合汁
数据 / 观察 · 01-06