数据 / 观察资讯
从14个衰老标志物视角,读懂“卵巢早衰”与“更年期”
2025-09-05 09:52 来源:新营养
衰老是每个人都无法回避的生命进程,而女性在衰老过程中,卵巢健康与更年期的到来更是备受关注的话题。2025年4月,索邦大学等研究团队将12个衰老标志物扩展到14个,让衰老机制的拼图更完整1。今天,我们就以这些标志物为钥匙,深入探讨其与卵巢早衰和女性更年期的奥秘。
01
先搞懂:14 个衰老标志物是什么?
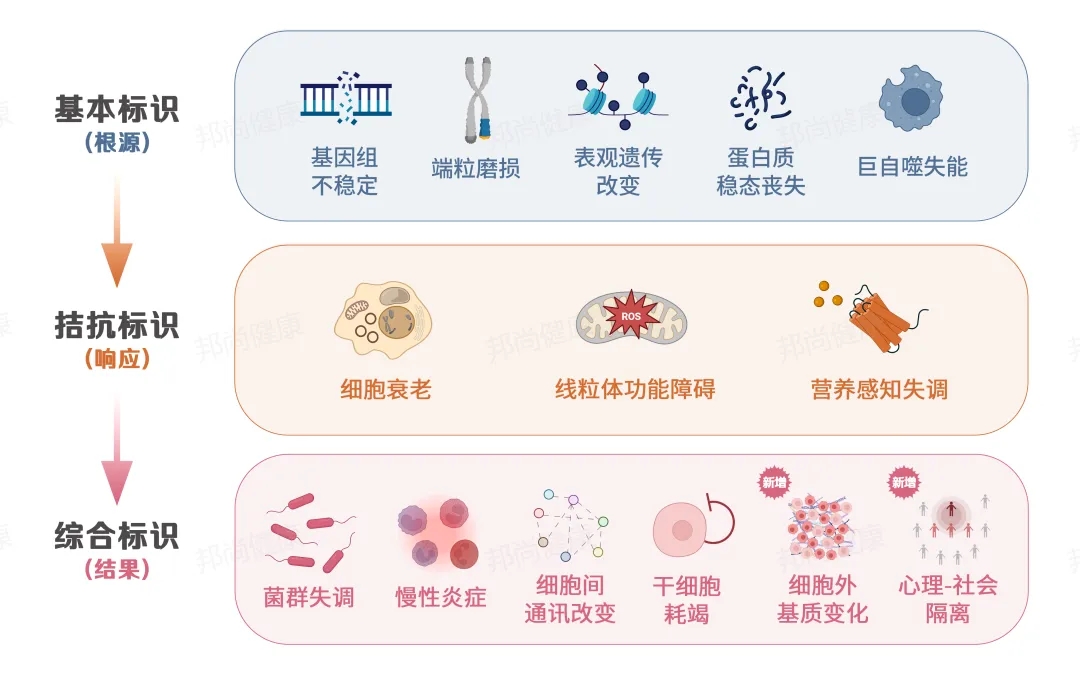
14 个衰老标志物并非杂乱无章,而是按照“根源-响应-结果”的逻辑,被划分为三大类,它们共同构成了衰老的“全景图”1,2:
基本标识:
衰老的“根本驱动力”
包括:基因组不稳定,端粒磨损,表观遗传改变,蛋白质稳态丧失,巨自噬失能。这些标志物是衰老发生的源头,就像机器运转的“核心零件故障”,直接触发衰老进程。
拮抗标识:
衰老的“应急响应与副作用”
包括:细胞衰老,线粒体功能障碍,营养感知失调。它们是身体对基本标志变化的“应对措施”,初衷是保护细胞,但长期激活或功能异常,反而会加剧衰老,也是我们理解卵巢问题的 “核心视角”。
综合标识:
衰老的“最终外在表现”
包括:菌群失调,慢性炎症,细胞间通讯改变,干细胞耗竭,细胞外基质变化(新增),心理社会隔离(新增)。它们是基本标识和拮抗标识长期作用的结果,直接体现为我们能观察到的衰老表型和慢性病风险,也是卵巢问题的“伴随信号”。
 图源:邦尚健康设计
图源:邦尚健康设计
02
聚焦卵巢健康:拮抗标识是“关键突破口”
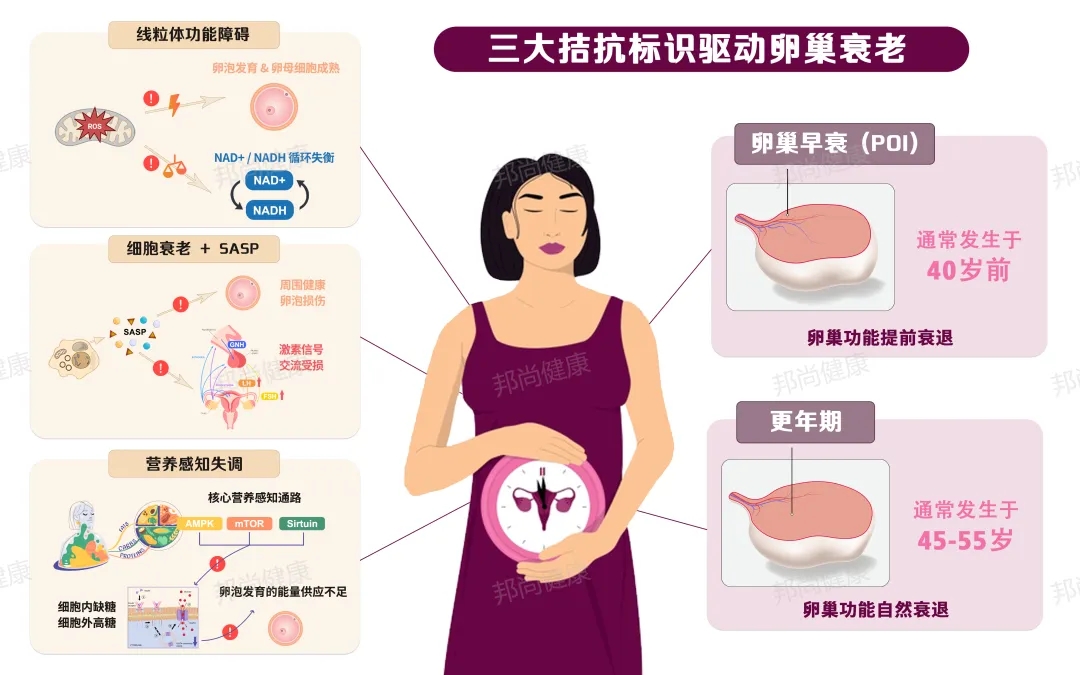
卵巢作为女性核心的内分泌与生殖器官,其功能维持与衰老进程密切相关。尤其在卵巢早衰(Premature Ovarian Insufficiency, POI,指40岁前卵巢功能衰退)和更年期(通常发生于45-55岁,卵巢功能自然衰退)的发生机制中,衰老生物学中提出的“拮抗标识”(Antagonistic Hallmarks)为我们提供了关键的解释框架和干预切入点 3。
卵巢早衰:拮抗标识 “提前失控”
卵巢早衰的本质,是卵巢细胞的“衰老程序提前启动”,而拮抗标识的异常是重要推手:
线粒体受损:
卵巢细胞的 “能量危机”
卵泡的发育、卵子的成熟都需要大量能量,线粒体是关键“供能者”。卵母细胞是人体中线粒体总数最多的细胞,可见其对能量的高度依赖。当线粒体因氧化损伤、基因突变等原因功能障碍时,卵泡细胞会陷入“能量不足”的困境 —— 无法完成正常的细胞分裂和分化,甚至提前凋亡。同时,线粒体功能障碍还会导致NAD+/NADH循环失衡(NAD+是能量代谢的关键辅酶),进一步加剧能量代谢紊乱,形成 “能量越缺,线粒体越差” 的恶性循环,最终导致卵泡储备快速耗竭,引发卵巢早衰。4
细胞衰老+SASP:
卵巢组织的“慢性污染”
卵巢中的免疫细胞(如巨噬细胞、T细胞)负责清除受损卵泡和衰老细胞。但随着年龄增长或外界刺激(如压力、环境污染),免疫细胞自身会先衰老,逐渐失去“清理能力”。这些未被清除的衰老细胞会在卵巢内堆积,持续释放 SASP——其中的炎症因子(如IL-6、TNF-α)会损伤周围健康卵泡,蛋白酶会破坏卵巢组织的细胞外基质,就像在卵巢里“埋了一堆定时炸弹”,不断破坏卵巢的微环境,加速卵巢功能衰退。5
营养感知失调:
“全身高糖,胰岛素抵抗”
营养感知通路(核心为AMPK、mTOR、sirtuin通路)是调控细胞代谢、衰老与生殖功能的关键 “信号开关”,营养感知通路失调导致细胞对营养信号敏感性下降,抑制胰岛素介导的葡萄糖转运蛋白(GLUT4)向细胞膜迁移,减少细胞对葡萄糖的摄取;此状态下,即使血液中葡萄糖充足,卵巢细胞也无法有效利用葡萄糖供能,导致 “细胞内缺糖,细胞外高糖”,从而直接影响卵泡发育的能量供应。同时营养感知失调会促进炎症介质(如TNF-α、IL-6)释放,进一步削弱胰岛素信号传导,导致胰岛素抵抗,这是发展成多囊卵巢综合征的核心因素。6
 图源:邦尚健康设计
图源:邦尚健康设计
03
女性更年期:拮抗标识“自然老化叠加”
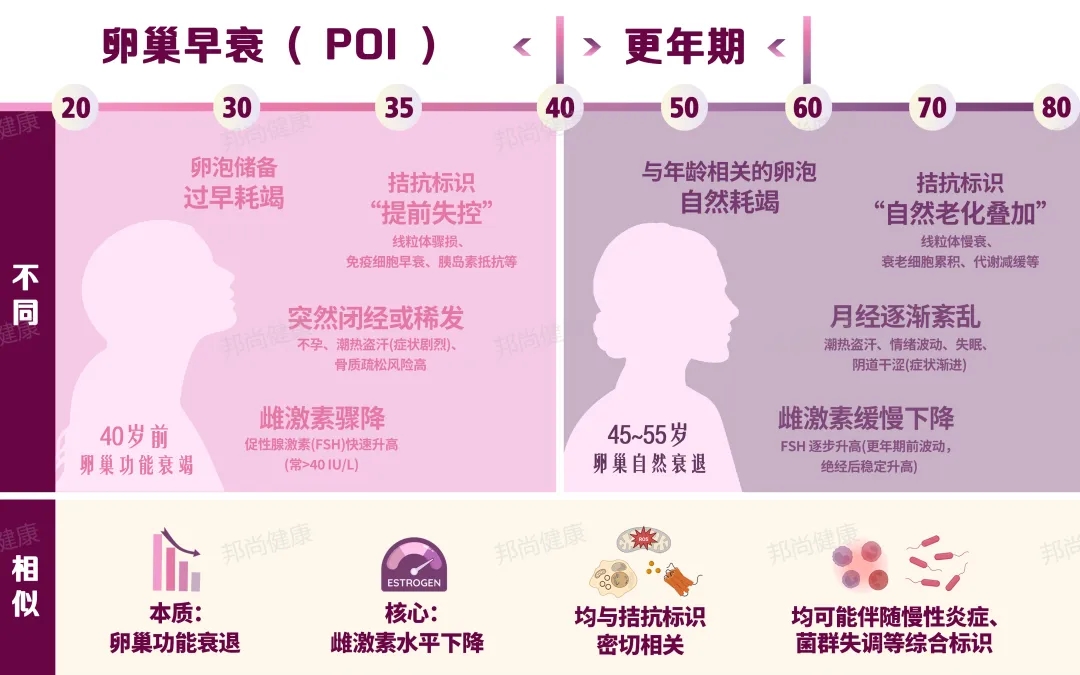
更年期是卵巢功能自然衰退的过程,本质是“基本标识长期作用后,拮抗标识全面失衡”的结果,与卵巢早衰的核心区别在于“进程速度”和“年龄节点”:
线粒体功能衰退:
从“故障”到“自然老化”
随着年龄增长(40岁后),线粒体的“自我修复能力”会逐渐下降,DNA突变积累、抗氧化酶活性降低,导致能量生产效率慢慢下降——不再是“突然故障”,而是 “逐渐减产”。这种缓慢的能量供应不足,会导致卵泡发育速度变慢、卵子质量下降,受精能力减弱,同时卵巢颗粒细胞(分泌雌激素的主要细胞)功能减弱,雌激素分泌逐渐减少,为更年期的到来埋下伏笔。7
细胞衰老累积:
从“局部污染”到“整体失衡”
更年期前,卵巢内的衰老细胞会被免疫细胞及时清理,SASP的影响相对有限;但45岁后,免疫细胞衰老速度加快,“清理能力” 赶不上“衰老细胞产生速度”,衰老细胞在卵巢内大量堆积,SASP的 “破坏力” 也从局部扩散到整体——不仅损伤卵泡,还会影响卵巢与下丘脑、垂体的激素通讯(比如雌激素对下丘脑的 “负反馈调节” 减弱),导致促性腺激素(FSH、LH)异常升高,引发月经紊乱、潮热、盗汗等更年期问题。5
营养感知失调:
从“功能异常”到“代谢适应”
更年期女性的营养感知失调,更多是“年龄相关的代谢减缓”与“激素变化”的叠加。营养感知失调(如sirtuin活性下调)会加速卵巢颗粒细胞衰老,缩短卵泡存活周期,提前耗尽卵泡储备,可能导致更年期提前到来。同时,通路失衡会加重更年期女性的代谢紊乱——雌激素下降本就易引发脂肪堆积,而通路失调进一步抑制AMPK介导的脂肪分解,促进mTOR驱动的脂肪合成,不仅加剧胰岛素抵抗风险,还会放大潮热、骨质疏松等更年期问题。6
 图源:邦尚健康设计
图源:邦尚健康设计
04
守护卵巢健康:”抗衰老” 营养素大盘点
针对卵巢早衰和更年期的核心机制,科学研究发现,以下营养素能从“修复线粒体、清除衰老细胞、调节营养感知、平衡激素水平”等角度,为卵巢健康提供支持:
非瑟酮:直击衰老细胞
非瑟酮是活性最强的 “衰老细胞清除剂(Senolytic)”天然黄酮之一。它的核心作用是,精准识别并诱导衰老细胞凋亡,减少卵巢内衰老细胞堆积,从而降低衰老细胞过量分泌的SASP对卵巢组织的损伤;同时,它能阻止衰老卵母细胞中关键抗衰蛋白Sirt1水平的下降,增强线粒体功能,恢复卵巢抗氧化能力,支持卵巢能量代谢状态,延缓卵巢衰老进程。8
尿石素A:支持线粒体能量代谢
尿石素A是目前公认的 “线粒体健康促进剂”,其被证实可以通过激活线粒体自噬通路(如PINK1/Parkin 信号轴)提高线粒体自噬水平,促进功能失调线粒体的选择性降解,同时维持线粒体生物合成与氧化呼吸功能,确保卵细胞能量供应。还可以显著影响卵巢组织形态学结构,提升卵泡储备,优化卵母细胞质量。9
S-雌马酚:双向平衡雌激素
S-雌马酚是大豆异黄酮在人体肠道内的活性代谢产物,其结构与人体雌激素相似,能双向温和调节雌激素水平。当体内雌激素不足时(如更年期、卵巢早衰),它能结合雌激素受体,发挥弱雌激素效应,缓解潮热、盗汗等情况;当体内雌激素过高时,能竞争性结合受体,避免雌激素过量刺激卵巢。10
黑姜提取物:聚焦胰岛素抵抗和营养感知
黑姜提取物的核心作用是影响胰岛素敏感性和能量代谢。它能激活AMPK信号通路(“能量传感器”),促进细胞对葡萄糖的吸收和利用,以影响胰岛素抵抗;同时可以通过抑制体重增加、阻断脂肪生成、促进脂肪分解及刺激产热等机制维持健康的体重和胰岛素敏感性。11
灵芝提取物:全方位守护卵巢健康
灵芝提取物(活性成分灵芝多糖、三萜类化合物)在传统中医中被视为 “滋补佳品”,现代研究也证实其对卵巢健康的多重保护作用,包括增强免疫细胞活性(如巨噬细胞、NK细胞),从而提升卵巢内衰老细胞的 “清理效率”,减少SASP堆积。其次,调节下丘脑-垂体-卵巢轴的激素平衡,抑制促性腺激素异常升高,缓解更年期情绪波动、月经紊乱等情况。12
 图源:邦尚健康设计
图源:邦尚健康设计
卵巢健康是女性衰老进程中的核心环节,14个衰老标志物为我们提供了科学的解读工具。无论是预防卵巢早衰,还是平稳度过更年期,除了合理补充营养素,规律作息、均衡饮食、适度运动(如瑜伽、快走,能改善卵巢血流)、管理压力(减少皮质醇对卵巢的损伤)同样重要。衰老不可逆转,但我们可以通过科学的方式,让卵巢衰退的脚步慢一点,让女性的生命质量更高一点。
参考文献:
1. Guido Kroemer, Andrea B Maier, et al. From geroscience to precision geromedicine: Understanding and managing aging. Cell, 2025 Apr 17;188(8):2043-2062.
2. Carlos López-Otín 1, Maria A Blasco, et al. Hallmarks of aging: An expanding universe. Cell. 2023 Jan 19;186(2):243-278.
3. Chuqing Wu, Dan Chen, et al. Hallmarks of ovarian aging. Trends Endocrinol Metab. 2025 May;36(5):418-439.
4. Jasmine L Chiang, Pallavi Shukla, et al. Mitochondria in Ovarian Aging and Reproductive Longevity. Ageing Res Rev. 2020 Nov:63:101168.
5. José V V Isola, Jessica D Hense, et al. Reproductive Ageing: Inflammation, immune cells, and cellular senescence in the aging ovary. Reproduction. 2024 Jun 21;168(2):e230499.
6. Chuqing Wu, Dan Chen, et al. Hallmarks of ovarian aging. Trends Endocrinol Metab. 2025 May;36(5):418-439.
7. Marcelo Borges Cavalcante, et al. Ovarian aging in humans: potential strategies for extending reproductive lifespan. Geroscience. 2023 Aug;45(4):2121-2133.
8. Xing X, Liang Y, et al. Fisetin Delays Postovulatory Oocyte Aging by Regulating Oxidative Stress and Mitochondrial Function through Sirt1 Pathway. Molecules. 2023 Jul 20; 28(14):5533.
9. Weiyong Wang, Ren Zhou, et al. Biology (Basel), Urolithin A Protects Ovarian Reserve Via Inhibiting PI3K/Akt Signaling and Preventing Chemotherapy-Induced Follicle Apoptosis. 2025 Jul 8;14(7):829.
10. Jing Lv, Shengkai Jin, et al. Equol: a metabolite of gut microbiota with potential antitumor effects. Gut Pathog. 2024 Jul 7;16:35.
11. Sun Pyo Kim, Inae Jeong, et al. Black Ginger Extract Suppresses Fat Accumulation by Regulating Lipid Metabolism in High-Fat Diet-Fed Mice. J Med Food. 2024 Oct;27(10):922-930.
12. Elif Ekiz, Emel Oz, et al. Exploring the Potential Medicinal Benefits of Ganoderma lucidum: From Metabolic Disorders to Coronavirus Infections. Foods 2023, 12(7), 1512
END
>>>声明
*新营养(xinyingyang.com)致力于秉承循征营养学的理念,重度垂直人类营养,为营养健康产业从业者架起沟通的桥梁,标明原创的文章权限为本网所有,如需转载请得到书面申请并在文章开头注明出处。
*文章中会充列示参考文献,但因商业利益相关造成的不客观可能依然存在,欢迎读者多提出批评意见和建议。
*文章中涉及功效信息内容均有对应的数据支持,囿于篇幅限制无法全部刊登,如需数据来源,可向新营养(xinyingyang.com)或文章中涉及到的企业索取。文章图片部分来源于网络,如有侵权请告知删除。
*此公众号中全部内容仅为创新案例的一般性参考。读者不应在缺乏具体的专业建议的情况下,擅自根据文章内容中的任何信息采取行动。此公众号运营方将不对任何因采用文章内容而导致的损失负责。
*文章中涉及的产品、成分、功效仅代表相关企业的观点,新营养仅基于信息传递目的进行转述,并不代表我们绝对认同相关宣称,也不支持任何产品的营销和销售。
*文章中插入的图片不涉及到商业行为,仅限交流,并标明了来源出处,尊重原创图片设计。
新营养留言互动
您的电话不会被公开。 必填项已用 * 标注
相关热词搜索:
上一篇:升级全链式服务,仙乐健康助力品牌找到五大高潜赛道的加速引擎
下一篇:新营养周报| 好丽友木糖醇3+迅醒无糖口香糖上新、宜品乳业递交上市申请、Food & Function:甘蔗多酚具有降尿酸活性
新营养峰会/活动
新营养热门资讯
共晶技术:让营养素步入埃米时代
XINGRAPHIC · 09-11
11月6-7日广州新营养趋势大会!30+演讲、2
风信社 · 09-08
当“造物”成为可能,人类营养健康产业将迎
XINGRAPHIC · 07-07
新营养周报 | 农夫山泉上新蓝靛果混合汁
数据 / 观察 · 01-06